
ACADÉMICO - CIENTÍFICA
¿SABÍA USTED COLEGA GINECO-OBSTETRA? ÚLTIMOS AVANCES Y NOVEDADES MÁS DESTACADAS EN GINECOLOGÍA
Nuevos productos para la menopausia, osteoporosis, VPH, endometriosis, cáncer de ovario y vejiga hiperactiva, y para evitar embarazos no deseados.
| Tomado de: https://farmacosalud.com/ultimos-avances-y-novedades-mas-destacadas-en-ginecologia/
Redacción Farmacosalud.com
A continuación, se señalan algunas de las novedades y avances más destacados de los últimos tiempos en el ámbito de la ginecología.
Llega Lenzetto, un pulverizador transdérmico para tratar la menopausia
Llega a España Lenzetto®, un pulverizador transdérmico para reducir los síntomas moderados y severos –sofocos, insomnio, irritabilidad y sequedad vaginal– durante la menopausia, mejorando la calidad de vida de las mujeres que los padecen. Este dispositivo único, innovador y de fácil uso, que ha lanzado Gedeon Richter al mercado, permite la administración transdérmica de una dosis baja de estradiol. Este pulverizador permite administrar una dosis exacta de estrógeno de una forma cómoda y precisa.
La sencillez de la aplicación contribuye a una mayor continuidad en el tratamiento, lo que mejora el grado de cumplimiento y reduce la tasa de abandonos. Lenzetto se administra haciendo una pulverización en la zona del antebrazo o en la parte interna del muslo las veces recomendadas. Se empieza con una pulverización, y si hiciera falta, se puede incrementar la dosis, siempre siguiendo las indicaciones del especialista tras evaluar cada caso.

Simbolsimo sobre las fases de la Menopausia
Fuente: Archivo
La menopausia es un estadio natural en la vida de la mujer que, aun no estando siempre relacionado con problemas de salud, puede producir un importante impacto en su calidad de vida. Durante la menopausia se produce un cese de la actividad ovárica y una disminución de la producción endógena de estrógeno. Este proceso se puede producir a partir de los 45 años, aunque es más frecuente que aparezca a partir de los 50 años. Un estudio realizado en varios países indica que dos tercios de las mujeres entre 40 y 55 años sufren, al menos, de algún síntoma, siendo los sofocos el más común.
Disponible en España Actonel semanal, indicado para la osteoporosis
Actonel semanal comprimidos gastrorresistentes ya está disponible en España. Se trata del primer y único risedronato oral que se puede tomar justo después del desayuno[1], ya que su absorción no se ve afectada por los alimentos. Hasta un 36% de los pacientes no respeta el tiempo de ayuno entre su bisfosfonato oral y el desayuno[2]. Gracias a la innovadora formulación de Actonel, el nuevo producto optimiza la absorción intestinal y la biodisponibilidad[1,3].
Una de las limitaciones que más afecta a la adherencia con los bisfosfonatos orales, grupo terapéutico más utilizado para el tratamiento de la osteoporosis, es la necesidad de ayuno tras la toma del comprimido[4]. Teva Pharmaceuticals ha desarrollado una formulación gastrorresistente de su Actonel® Semanal (risedronato 35 mg) que puede tomarse junto con el desayuno. El producto está siendo promocionado por Theramex en España.
La absorción de Actonel Semanal 35 mg Comprimidos Gastrorresistentes no se ve afectada por los alimentos gracias a su revestimiento único sensible al pH4 con una dispersión acuosa avanzada de copolímero aniónico, por lo que la liberación y absorción del principio activo tienen lugar en el intestino delgado. Además, en su formulación contiene también ácido etilendiaminotetraacético (EDTA), un agente quelante de calcio, que permite eliminar la necesidad de tomar la medicación en ayunas sin afectar la biodisponibilidad de Risedronato o su eficacia.[3,4] Actonel® Semanal 35 mg Comprimidos Gastrorresistentes presenta una alternativa terapéutica para los pacientes en tratamiento para la osteoporosis, manteniendo además el mismo precio[5] que el del resto de risedronatos semanales que están actualmente en el mercado.
Luz verde a Gardasil 9, la primera vacuna nonavalente antiVPH
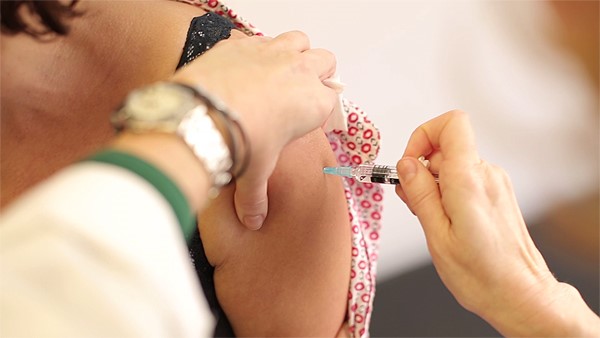
Autor/a de la imagen: Enric Arandes
Fuente: E. Arandes / www.farmacosalud.com
Gardasil® 9 (de la compañía MSD), la primera vacuna nonavalente que protege del Virus del Papiloma Humano (VPH), ha sido aprobada en España. Está indicada para toda la población a partir de los 9 años de edad, básicamente porque se ha demostrado que es efectiva independientemente de la edad y del sexo de las personas vacunadas. El nuevo preparado vacunal protege frente a nueve tipos distintos del Virus del Papiloma Humano, en concreto los tipos 6, 11, 16, 18, 31, 33, 45, 52, 58. De esta manera, la nueva vacuna protege frente a cinco tipos de VPH más que las vacunas existentes hasta ahora, tratándose de la única nonavalente disponible frente al VPH[6]. Este virus es causa necesaria para que se produzca el cáncer cervical, pero a la vez se encuentra implicado en un elevado número de cánceres genitales y extragenitales como vagina, vulva, ano, pene, y en menor medida en cánceres del área orofaríngea.
Los 9 tipos incluidos en la vacuna nonavalente son responsables del 90% de los cánceres cervicales, del 85-90% de los cánceres vulvares relacionados con el VPH, del 80-85% de cánceres vaginales relacionados con el VPH, y del 90-95% de cánceres anales relacionados con el VPH. Además, estos tipos también son responsables del 75-85% de las neoplasias cervicales intraepiteliales (CIN 2/3) de alto grado y de la mayor parte de las displasias vulvares, vaginales y anales relacionadas con este virus. No hay que olvidar tampoco la implicación de los tipos 16 y 18 en el 90% de las verrugas genitales.
Los estudios realizados han determinado que los niveles de anticuerpos conseguidos con Gardasil 9 son similares en niñas de 9 a 14 años, niños de esta misma edad o varones hasta 26 años si se compara con el grupo de mujeres de hasta 26 años, que constituyen la referencia en estos ensayos. En todos los grupos, la población vacunada ha presentado respuesta de anticuerpos al ser vacunados con la nonavalente. Estos resultados demuestran que la protección frente al VPH es efectiva en todos los grupos, independientemente de la edad y del sexo. La pauta de vacunación es de 2 o 3 dosis en función de la edad de la persona a proteger.
Orilissa, aprobada como terapia para el dolor asociado a la endometriosis

Fuente: Archivo
AbbVie, en cooperación con Neurocrine Biosciences, ha anunciado que la FDA (Estados Unidos) ha dado el visto bueno a ORILISSA™ (elagolix), el primer tratamiento oral aprobado por la FDA para el tratamiento del dolor -de moderado a severo- asociado con la endometriosis en más de una década. Los datos de los ensayos clínicos demostraron que ORILISSA redujo significativamente los tres tipos más comunes de dolor por endometriosis: dolor pélvico menstrual diario, dolor pélvico no menstrual y dolor con el sexo. Las mujeres fueron tratadas con ORILISSA 150 mg una vez al día y 200 mg dos veces al día.
La endometriosis se define como la presencia de tejido endometrial fuera del útero, lo que induce una reacción inflamatoria. Es una enfermedad crónica cuya causa se desconoce, aunque se ha comprobado una predisposición genética. Se estima que la endometriosis afecta al 7-15% de las mujeres en edad fértil[7].
Aunque en ocasiones las mujeres con endometriosis no presentan síntomas, es frecuente que refieran menstruaciones dolorosas (dismenorrea), relaciones sexuales dolorosas (dispareunia), reglas más abundantes, problemas de fertilidad o fatiga. Si afecta a la vejiga o al intestino pueden manifestar dolor con las deposiciones o molestias miccionales[8]. Las pruebas diagnósticas más frecuentes para detectar la endometriosis son tres en total: la exploración pélvica, la ecografía transvaginal y la laparoscopia pélvica[9].
AstraZeneca y MSD co-promocionan Lynparza
AstraZeneca y MSD han firmado un acuerdo estratégico de colaboración en oncología con el objetivo de co-promocionar Lynparza® (olaparib), el primer inhibidor de la poli ADP-ribosa polimerasa (PARP) aprobado a nivel mundial. Esta alianza permitirá poner a disposición de un mayor número de pacientes los tratamientos más innovadores que suponen una diferencia real en su calidad de vida. En España, olaparib está aprobado como monoterapia para el tratamiento de mantenimiento de pacientes adultos con cáncer de ovario epitelial seroso de alto grado, de trompa de Falopio, o peritoneal primario, con mutación genética BRCA (germinal y/o somática), sensible a platino, en recaída, que están en respuesta (respuesta completa o parcial) a quimioterapia basada en platino[10]. Recientemente, la EMA ha otorgado la autorización de olaparib en comprimidos para el tratamiento de cáncer de ovario en recaída sensible a platino con independencia del estado mutacional del gen BRCA[11].
Olaparib es un inhibidor del PARP, el primero de su clase autorizado para cáncer de ovario avanzado y recientemente fue autorizado por la FDA para el tratamiento de pacientes con cáncer de mama metastásico Her2- y mutación BRCA. Con este inhibidor del PARP se han tratado más de 20.000 pacientes en todo el mundo y cuenta con un amplio y avanzado programa de desarrollo clínico con 14 indicaciones en investigación para diversos tipos de tumores, que incluyen el cáncer de mama, de próstata y páncreas, entre otros.
Llega Mictonorm, indicado para incontinencia derivada de la VH

Fuente: Archivo
Lacer ha lanzado en España Mictonorm 30 mg (propiverina), un fármaco indicado para la incontinencia urinaria en pacientes con vejiga hiperactiva (VH). Propiverina es eficaz en el tratamiento sintomático de la incontinencia urinaria y/o incremento de la frecuencia y urgencia urinarias en pacientes con síndrome de VH. La vejiga hiperactiva es una enfermedad muy prevalente -afecta a más de 400 millones de personas en el mundo-, pero que, sin embargo, está infradiagnosticada. El principal síntoma es la urgencia urinaria, que limita la autonomía y deteriora sensiblemente la calidad de vida.
Propiverina presenta un doble mecanismo de acción: antimuscarínico y modulador de los canales de calcio. Este calcio es indispensable para que el músculo detrusor se contraiga y provoque la expulsión de la orina. La VH está causada, en la mayoría de las ocasiones, por la aparición de contracciones involuntarias del músculo detrusor. De ahí la importancia de la propiverina, ya que, aunque pertenece a la familia de los antimuscarínicos, se diferencia por su acción dual: no solo bloquea los receptores muscarínicos, como cualquier otro anticolinérgico, sino que, además, impide la entrada de calcio en las células del músculo detrusor. Así, este fármaco estabiliza dicho músculo e inhibe las contracciones por distintos estímulos, disminuyendo así el número de micciones y los episodios de incontinencia y de emergencia en 24 horas. Esta terapia presenta una farmacocinética lineal y una semivida de 15 horas, lo que permite la toma de una dosis al día. Propiverina se asocia a un riesgo de abandono del tratamiento menor en comparación con otros anticolinérgicos[12].
Setlona, un anticonceptivo que aumenta la adherencia terapéutica
La compañía Mylan ha puesto en el mercado Setlona, un anillo vaginal anticonceptivo de última generación que permite una mayor accesibilidad gracias a su menor precio. Esta circunstancia de tipo económico, junto con la ventaja que representa que el nuevo dispositivo no requiera condiciones especiales de conservación y que su composición evite el ‘estallido’ de liberación de hormonas en el torrente circulatorio, redunda en un mejor cumplimiento anticonceptivo.
Setlona presenta una reducción de precio del 25% frente a la presentación de tres anillos más barata existente en el mercado. Con Setlona, además, se evitan algunos de los efectos secundarios de los anillos vaginales clásicos, como son una mayor sensación de molestia en el pecho, náuseas e incluso algún pequeño vómito. El nuevo anticonceptivo está disponible en presentaciones de uno y tres anillos[13].
Referencias:
- Ficha técnica Actonel® 35 mg comprimidos gastrorresistentes.
- Vytrisalov M. et al. Climateric 2015; 18: 608-616.
- McClung M.R. et al. Osteoporosis Int 2013; 24: 301-310.
- Pazianas M. et al. Therapeutics and Clinical Risk Management 2013; 9: 395 – 402.
- Nomenclátor: https://www.mscbs.gob.es/ca/profesionales/nomenclator.do
- Ficha técnica de Gardasil 9.
- Agencia de Evaluación de Tecnologías Sanitarias (AETS). Instituto de Salud Carlos III. Ministerio de Sanidad. ‘ENDOMETRIOSIS. Revisión de la evidencia científica’. 2007. https://www.mscbs.gob.es/organizacion/sns/planCalidadSNS/pdf/equidad/informeEvidenciaEndometriosis70308.pdf
- Somdex Ginecología. ‘Endometriosis’. http://www.santiagodexeus.com/es/ginecologia/patologias/endometriosis/
- Barcelona IVF. ‘Endometriosis: Aprende a detectar sus síntomas’. 2016. https://barcelonaivf.com/endometriosis-y-sus-sintomas/
- Ficha técnica Lynparza (olaparib). Disponible en AEMPS: https://www.aemps.gob.es/cima/pdfs/es/p/114959001/114959001_p.pdf
- CHMP assessment report on extension of marketing authorisation grouped with a variation. Disponible en EMA: http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Assessment_Report_-_Variation/human/003726/WC500249582.pdf
- www.farmacosalud.com. ‘Avances en vejiga hiperactiva. Nuevos fármacos’. Drs. Martínez-Berganza, Brenes y Salinas, y el Prof. Tamargo. VI Jornadas Nacionales Nefrourológicas de SEMERGEN. 2018. http://www.farmacosalud.com/avancesenvejigahiperactivanuevosfarmacosSEMERGEN.pdf
- www.farmacosalud.com. ‘Llega un anillo vaginal anticonceptivo que aumenta la adherencia terapéutica’. Declaraciones del Dr. Sánchez Borrego. 2018. http://farmacosalud.com/llega-setlona-un-anillo-vaginal-anticonceptivo-que-aumenta-la-adherencia-terapeutica/

